Cryo-electron microscopy
این میکروسکوپ که به طور خلاصه به صورت cryo-em گفته می شود شکلی از میکروسکوپ TEM (و یا به عبارتی transmission electron microscopy) می باشد که جهت تصویر برداری مولکولیهای زیستی در دماهای cryogenic مورد استفاده قرار میگیرد.
دماهایی cryogenic: در علم فیزیک به مطالعه رفتار مواد در دماهای پایین cryogenic گفته می شود. و تقریبا به دمای کمتر از منفی 150 درجه سانتیگراد دمای cryogenic اطلاق می گردد.
در علم بیولوژی برای مطالعه ساختار مولکول های بزرگ مانند ریبوزوم ها، میتوکندی ها و ... از این میکروسکوپ استفاده می شود و محیطی که برای ایجاد دمای cryogenic مورد استفاده قرار میگیرد اکثرا نیتروژن مایع می باشد.
در حال حاضر این دقت (resolution) این تکنیک به طور پیوسته در حال افزایش می باشد.
@computational_science
این میکروسکوپ که به طور خلاصه به صورت cryo-em گفته می شود شکلی از میکروسکوپ TEM (و یا به عبارتی transmission electron microscopy) می باشد که جهت تصویر برداری مولکولیهای زیستی در دماهای cryogenic مورد استفاده قرار میگیرد.
دماهایی cryogenic: در علم فیزیک به مطالعه رفتار مواد در دماهای پایین cryogenic گفته می شود. و تقریبا به دمای کمتر از منفی 150 درجه سانتیگراد دمای cryogenic اطلاق می گردد.
در علم بیولوژی برای مطالعه ساختار مولکول های بزرگ مانند ریبوزوم ها، میتوکندی ها و ... از این میکروسکوپ استفاده می شود و محیطی که برای ایجاد دمای cryogenic مورد استفاده قرار میگیرد اکثرا نیتروژن مایع می باشد.
در حال حاضر این دقت (resolution) این تکنیک به طور پیوسته در حال افزایش می باشد.
@computational_science
#داروهای_پپتیدی
Development of Protein Mimics for Intracellular Delivery:
پیشرفت و استفاده از مقلدهای پروتئینی(داربست های پروتئینی) برای تحویل و انتقال مواد به داخل سلول:
استفاده از پپتید ها به عنوان دارو امروزه به صورت رایج در حال انجام است. مبحث بعدی در این حیطه استفاده از پپتید ها و پروتئین ها به عنوان حامل دارو است. ولی وقتی پپتید ها به عنوان حامل استفاده می شوند باید ثبات دارو، حفظ حلالیت دارو و تحویل و آزادسازی دارو را فراهم سازند. که از بین این موارد رهاسازی دارو در بافت هدف به صورت کارآمد و تحویل دارو به داخل سلول از اهمیت زیادی برخوردار است.لذا برای رسیدگی به این مشکلات گروهی از محققان از طبیعت الهام گرفته اند.در واقع می توان از پروتئین هایی که شکل مناسب دارند و قادر به عبور از غشائ سلولی هستند به عنوان حامل داروها و پپتید ها استفاده کرد. در شکل زیر دو نمونه از این پروتئین ها را مشاهده می کنیم.
@computational_science
Development of Protein Mimics for Intracellular Delivery:
پیشرفت و استفاده از مقلدهای پروتئینی(داربست های پروتئینی) برای تحویل و انتقال مواد به داخل سلول:
استفاده از پپتید ها به عنوان دارو امروزه به صورت رایج در حال انجام است. مبحث بعدی در این حیطه استفاده از پپتید ها و پروتئین ها به عنوان حامل دارو است. ولی وقتی پپتید ها به عنوان حامل استفاده می شوند باید ثبات دارو، حفظ حلالیت دارو و تحویل و آزادسازی دارو را فراهم سازند. که از بین این موارد رهاسازی دارو در بافت هدف به صورت کارآمد و تحویل دارو به داخل سلول از اهمیت زیادی برخوردار است.لذا برای رسیدگی به این مشکلات گروهی از محققان از طبیعت الهام گرفته اند.در واقع می توان از پروتئین هایی که شکل مناسب دارند و قادر به عبور از غشائ سلولی هستند به عنوان حامل داروها و پپتید ها استفاده کرد. در شکل زیر دو نمونه از این پروتئین ها را مشاهده می کنیم.
@computational_science
#داروهای_پپتیدی
در شکل بالا یکی پروتئین HIV-1 TAT است و دیگری پروتئین antennapedia homeodomainاست. در واقع در این روش از قالب ساختاری پروتئین های مورد نظر به عنوان داربست استفاده می شود و دارو یا پپتید بر روی این داربست قرار می گیرد و چون پروتئین مورد نظر ما به صورت طبیعی دارای خاصیت عبور از غشاء سلولی می باشد وقتی که به بافت هدف می رسد می تواند دارو یا پپتید مورد نظر را از داخل غشاء عبور دهد و داخل سلول آزاد کند. در شکل زیر نیز تعدادی از مقلد ها یا داربست های پروتئیینی که در طی الیان متوالی و به ترتیب پیشرفت کرده اند را مشاهده میکنیم.
@computational_science
در شکل بالا یکی پروتئین HIV-1 TAT است و دیگری پروتئین antennapedia homeodomainاست. در واقع در این روش از قالب ساختاری پروتئین های مورد نظر به عنوان داربست استفاده می شود و دارو یا پپتید بر روی این داربست قرار می گیرد و چون پروتئین مورد نظر ما به صورت طبیعی دارای خاصیت عبور از غشاء سلولی می باشد وقتی که به بافت هدف می رسد می تواند دارو یا پپتید مورد نظر را از داخل غشاء عبور دهد و داخل سلول آزاد کند. در شکل زیر نیز تعدادی از مقلد ها یا داربست های پروتئیینی که در طی الیان متوالی و به ترتیب پیشرفت کرده اند را مشاهده میکنیم.
@computational_science
از دوستان عزیز تقاضا دارم حتما مطالب مربوط به داروهایی پپتیدی را پیوسته مطالعه و دنبال کنند، چون هدف ما از ارائه این مطالب ایجاد دیدی متفاوت در دنیای پپتیدها می باشد، و سعی ما بر این است که مطالب و مقاله های روز در حوزه داروهای پپتیدی را به فراهم کنیم تا در ارائه ایده های جدید به دوستان کمکی حتی کوچک کرده باشیم. با تشکر🙏
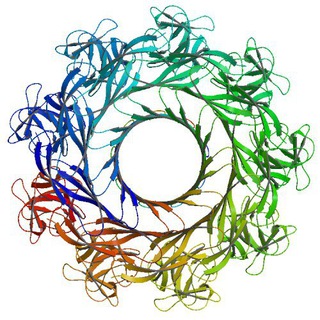
Cryo-EM structure of the Lysenin Pore @computational_science
فایل زیر هم تصویر 3 بعدی EM مربوط به عکس بالاست. جهت مشاهده آن می توانید از نرم افزار CHIMERA استفاده کنید.
Forwarded from ammar Mohseni
دوستانی که در زمینه دیتاماینینگ کار میکنن کتاب زیر رو حتما یه مطالعه ای بفرمایند. کتابی کم حجم اما مفید
Forwarded from کانال آموزش اکسل
Chemometrics in Excel-Wiley.pdf
6.5 MB
#داروهای_پپتیدی
Peptide Library: Open the door to new drug candidates
کتابخانه پپتیدی یک منبع اطلاعات از مجموعه پپتید های طراحی و سنتز شده است. لذا با استفاده از کتابخانه پپتیدی به راحتی می توان به نوع پپتیدی که نیاز داریم دسترسی پیدا می کنیم. یا می توانیم در این دیتا بیس پپتیدی که شبیه پپتید ما است را پیدا کنیم. علاوه بر این با استفاده از کتابخانه پپتیدی اصول طراحی و سنتز پپتید ها به عنوان دارو را نیز فرا بگیریم. زیرا پروتوکل و روش طراحی پپتید ها در این کتابخانه وجود دارد.
@computational_science
کتابخانه های پپتیدی انواع مختلفی دارند که شامل موار زیر می شود:
• Overlapping Peptide Library
• Truncation Peptide Library
• Alanine Peptide Scanning Library
• Random Peptide Library
• Scrambled Peptide Library
• Positional Peptide Library
یکی از کتابخانه های پپتیدی که وجود دارد وب سایت lifetein است. http://www.lifetein.com
اصولی که این گروه تحقیقاتی برای سنتز و طراحی پپتید ها و سپس ثبت آن در کتابخانه ها استفاده می کند تقریبا شبیه سایر کتابخانه های پپتیدی است. کتابخانه lifetein بر این اساس کار می کند که ابتدا پپتید ها طراحی و سنتز می شوند، بعد پپتید های سنتز شده اپتیمایز می شوند و در نهایت سنجش آنزیمی بر روی این پپتید ها صورت می گیرد و سپس پپتید هایی که مناسب هستند انتخاب می شوند و در کتابخانه ثبت می شوند.
@computational_science
Peptide Library: Open the door to new drug candidates
کتابخانه پپتیدی یک منبع اطلاعات از مجموعه پپتید های طراحی و سنتز شده است. لذا با استفاده از کتابخانه پپتیدی به راحتی می توان به نوع پپتیدی که نیاز داریم دسترسی پیدا می کنیم. یا می توانیم در این دیتا بیس پپتیدی که شبیه پپتید ما است را پیدا کنیم. علاوه بر این با استفاده از کتابخانه پپتیدی اصول طراحی و سنتز پپتید ها به عنوان دارو را نیز فرا بگیریم. زیرا پروتوکل و روش طراحی پپتید ها در این کتابخانه وجود دارد.
@computational_science
کتابخانه های پپتیدی انواع مختلفی دارند که شامل موار زیر می شود:
• Overlapping Peptide Library
• Truncation Peptide Library
• Alanine Peptide Scanning Library
• Random Peptide Library
• Scrambled Peptide Library
• Positional Peptide Library
یکی از کتابخانه های پپتیدی که وجود دارد وب سایت lifetein است. http://www.lifetein.com
اصولی که این گروه تحقیقاتی برای سنتز و طراحی پپتید ها و سپس ثبت آن در کتابخانه ها استفاده می کند تقریبا شبیه سایر کتابخانه های پپتیدی است. کتابخانه lifetein بر این اساس کار می کند که ابتدا پپتید ها طراحی و سنتز می شوند، بعد پپتید های سنتز شده اپتیمایز می شوند و در نهایت سنجش آنزیمی بر روی این پپتید ها صورت می گیرد و سپس پپتید هایی که مناسب هستند انتخاب می شوند و در کتابخانه ثبت می شوند.
@computational_science
Lifetein
Custom Peptide Synthesis Service - LifeTein
LifeTein offers custom peptide synthesis services, PNA, custom protein and antibody services at competitive price and fast turnaround time.
#داروهای_پپتید ساخت کتابخانه های پپتیدی @computational_science
#داروهای_پپتیدی
Activable Cell-Penetrating Peptide Conjugated Prodrug for Tumor Targeted Drug Delivery
در این مقاله یک پپتید فعال شونده دارای خاصیت نفوذپذیری به نام (CR8G3PK6, ACPP) با یک گروه محافظ به نام 2,3- dimethylmaleic anhydride (DMA)پوشانده شده و با داروی ضد تومور (DOX) کانژوگه و ترکیب شده است . این روش جدید در تکنولوژی دارورسانی برای اولین بار مورد استفاده قرار می گیرد و برای حمل داروهای ضد سرطانی که نیاز است وارد سلول شوند کاربرد دارد. این روش به طور کلی و در اصطلاح روش (DOX-ACPP-DMA) نامیده می شود. در واقع در این روش از خاصیت نفوذپذیری پپتید مورد نظر برای انتقال دارو به داخل سلول استفاده می شود. در این روش و همانطور که در شکل زیر مشخص است ابتدا کمپلکس مورد نظر که شامل دارو، پپتید و ترکیب پوشاننده است سنتز می شود. حامل مورد نظر به بدن فرد بیمار تجویز می شود و وارد جریان خون می شود در جریان خون PH معادل 7.4 است که باعث می شود پپتید موجود در کمپلکس حامل در فرم غیر فعال خود باشد. بعد از اینکه حامل وارد فضای بین سلولی سلول های سرطانی می شود و چون PH معادل 6.8 است پپتید فعال می شود و چون دارای خاصیت نفوذ از غشای سلولی است می تواند وارد سلول سرطانی شود و همراه خود دارو را نیز وارد سلول کند. بعد از ورود کمپلکس حامل به داخل سلول بلافاصله کمپلکس حامل(پپتید) توسط پروتئاز های سلولی تجزیه می شود و دارو (DOX) آزاد می شود.
@computational_science
Activable Cell-Penetrating Peptide Conjugated Prodrug for Tumor Targeted Drug Delivery
در این مقاله یک پپتید فعال شونده دارای خاصیت نفوذپذیری به نام (CR8G3PK6, ACPP) با یک گروه محافظ به نام 2,3- dimethylmaleic anhydride (DMA)پوشانده شده و با داروی ضد تومور (DOX) کانژوگه و ترکیب شده است . این روش جدید در تکنولوژی دارورسانی برای اولین بار مورد استفاده قرار می گیرد و برای حمل داروهای ضد سرطانی که نیاز است وارد سلول شوند کاربرد دارد. این روش به طور کلی و در اصطلاح روش (DOX-ACPP-DMA) نامیده می شود. در واقع در این روش از خاصیت نفوذپذیری پپتید مورد نظر برای انتقال دارو به داخل سلول استفاده می شود. در این روش و همانطور که در شکل زیر مشخص است ابتدا کمپلکس مورد نظر که شامل دارو، پپتید و ترکیب پوشاننده است سنتز می شود. حامل مورد نظر به بدن فرد بیمار تجویز می شود و وارد جریان خون می شود در جریان خون PH معادل 7.4 است که باعث می شود پپتید موجود در کمپلکس حامل در فرم غیر فعال خود باشد. بعد از اینکه حامل وارد فضای بین سلولی سلول های سرطانی می شود و چون PH معادل 6.8 است پپتید فعال می شود و چون دارای خاصیت نفوذ از غشای سلولی است می تواند وارد سلول سرطانی شود و همراه خود دارو را نیز وارد سلول کند. بعد از ورود کمپلکس حامل به داخل سلول بلافاصله کمپلکس حامل(پپتید) توسط پروتئاز های سلولی تجزیه می شود و دارو (DOX) آزاد می شود.
@computational_science
#داروهای_پپتیدی
A Web Server and Mobile App for Computing Hemolytic Potency of Peptides
تعداد زیادی از داروهای پپتیدی که سنتز می شوند فقط به این دلیل وارد فاز کلینیکال و درمانی نمیشوند که فعالیت همولایتیکی ( hemolytic activity) بالایی دارند. لذا در این تحقیق دیتابیسی طراحی و پیشرفت داده شده است که پپتید هایی که فعالیت همولایتیک مناسب دارند را از پپتید هایی که فعالیت همولایتیکی مناسب ندارند جدا می کند. همچنین در کناراین وب سرور یک اپلیکشن موبایل نیز طراحی شده است که پپتید هایی که پتانسیل همولایتیک بالایی دارند را پیشگویی و screening می کند. در ابتدا دیتابیسی طراحی شده است که HemoPI-1 that نامیده میشود و حاوی 552 نمونه همولایتیک و 552 نمونه غیرهمولایتیک است. سپس آنالیزهای بعدی بر روی توالی این نمونه ها نشان داد که رزیدوهای خاصی مثل (e.g., L, K, F, W) و موتیف های (e.g., “FKK”, “LKL”, “KKLL”, “KWK”, “VLK”, “CYCR”, “CRR”, “RFC”, “RRR”, “LKKL”) بیشتر در پپتید های همولایتیک وجود دارند. بنابراین مدل های پیشرفته ای برای پپتید های همولایتیک و غیر همولایتیک با استفاده از تکنیک های یادگیری ماشین به دست آمده است که accuracy آن بیشتر از 95% است. همچنین در این تحقیق مدل های پیشرفته ایی برای پپتید هایی که پتانسیل همولایتیک پایین یا بالا دارند نیز به صورت دیتابیس طراحی شده اند که به ترتیب HemoPI-2 و HemoPI-3 نامیده می شوند. برای مثال در شکل زیر مثالی از نمونه های همولایتیک و غیر همولایتیک را برای HemoPI-2 dataset مشاهده میکنیم. برای کسب اطلاعات بیشتر می تواند این مقاله را به صورت کامل مطالعه فرمایید.
@computational_science
A Web Server and Mobile App for Computing Hemolytic Potency of Peptides
تعداد زیادی از داروهای پپتیدی که سنتز می شوند فقط به این دلیل وارد فاز کلینیکال و درمانی نمیشوند که فعالیت همولایتیکی ( hemolytic activity) بالایی دارند. لذا در این تحقیق دیتابیسی طراحی و پیشرفت داده شده است که پپتید هایی که فعالیت همولایتیک مناسب دارند را از پپتید هایی که فعالیت همولایتیکی مناسب ندارند جدا می کند. همچنین در کناراین وب سرور یک اپلیکشن موبایل نیز طراحی شده است که پپتید هایی که پتانسیل همولایتیک بالایی دارند را پیشگویی و screening می کند. در ابتدا دیتابیسی طراحی شده است که HemoPI-1 that نامیده میشود و حاوی 552 نمونه همولایتیک و 552 نمونه غیرهمولایتیک است. سپس آنالیزهای بعدی بر روی توالی این نمونه ها نشان داد که رزیدوهای خاصی مثل (e.g., L, K, F, W) و موتیف های (e.g., “FKK”, “LKL”, “KKLL”, “KWK”, “VLK”, “CYCR”, “CRR”, “RFC”, “RRR”, “LKKL”) بیشتر در پپتید های همولایتیک وجود دارند. بنابراین مدل های پیشرفته ای برای پپتید های همولایتیک و غیر همولایتیک با استفاده از تکنیک های یادگیری ماشین به دست آمده است که accuracy آن بیشتر از 95% است. همچنین در این تحقیق مدل های پیشرفته ایی برای پپتید هایی که پتانسیل همولایتیک پایین یا بالا دارند نیز به صورت دیتابیس طراحی شده اند که به ترتیب HemoPI-2 و HemoPI-3 نامیده می شوند. برای مثال در شکل زیر مثالی از نمونه های همولایتیک و غیر همولایتیک را برای HemoPI-2 dataset مشاهده میکنیم. برای کسب اطلاعات بیشتر می تواند این مقاله را به صورت کامل مطالعه فرمایید.
@computational_science
Two sample logos of hemolytic and non-hemolytic peptides of HemoPI-2 dataset @computational_science
Forwarded from Bioinformatics & Computational Biology
شبیه سازی دینامیک مولکولی ، طراحی پپتید و داروهای هدفمند
لینک گروه و کانال تخصصی بیولوژی محاسباتی و بیوانفورماتیک
https://telegram.me/joinchat/BP7D2zyFRAJTZgcOxXJA9A
@computational_science
لینک گروه و کانال تخصصی بیولوژی محاسباتی و بیوانفورماتیک
https://telegram.me/joinchat/BP7D2zyFRAJTZgcOxXJA9A
@computational_science